
Буферные смеси и регулировка pH в аквариуме - тема, где маркетинг часто побеждает здравый смысл. Многие аквариумисты сначала борются с "неправильным" pH бутылочками, а уже потом узнают, что сама идея "поднять pH химией" часто ведет к откатам и стрессу рыб, потому что в системе игнорируется главный игрок - буферная емкость воды.
Что такое pH и почему он вообще "скачет"

pH - это мера кислотности воды, то есть концентрации ионов водорода H+. Его удобно представлять не как "магическую цифру", а как баланс между кислотами и основаниями.
В аквариуме на pH влияют: растворенный CO2, карбонатная жесткость (KH), органика, подмены и добавки. Без понимания KH любые попытки управлять pH сильными кислотами или щелочами работают как "дернуть качели" - краткий эффект, а потом возврат.
Кислоты и щелочи - прямой удар
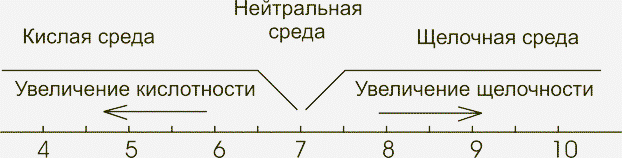
Кислота (например, соляная, фосфорная) при добавлении в воду "съедает" часть карбонатного буфера и понижает pH за счет увеличения концентрации H+.
Щелочь (например, сода, гидроксид натрия) связывает H+ и сдвигает pH вверх. Это прямое изменение баланса, но не создание стабильности.
Когда в аквариуме мало буфера (низкий KH), даже небольшое количество кислоты или щелочи может сильно сместить pH. Внешне это похоже на "отлично, сработало", но такая система становится крайне чувствительной к любым изменениям: дыхание рыб и бактерий, ночные колебания CO2, подмены воды.
Что такое буфер и буферная смесь

Буфер - это система из слабой кислоты и ее соли (или слабого основания и его соли), которая "ловит" изменения pH, не давая ему сильно смещаться.
Классический природный буфер в аквариуме - карбонатная система: углекислый газ, угольная кислота, гидрокарбонаты и карбонаты. Именно она в большинстве пресноводных аквариумов определяет KH и устойчивость pH.
Буферная смесь в аквариумистике - это препарат (или комбинация веществ), который не просто разово сдвигает pH, а задает новый стабильный диапазон, в котором вода "сопротивляется" изменениям. В отличие от "голой" кислоты или щелочи, буфер не просто меняет цифру, а создает систему, которая удерживает ее.
Главные отличия кислот/щелочей от буферов
- Направление действия:
- Кислоты/щелочи - это однократный сдвиг pH здесь и сейчас.
- Буфер - это создание устойчивого "коридора" pH, который держится даже при небольших внешних воздействиях.
- Поведение во времени:
- После добавления кислоты/щелочи pH сначала резко меняется, а потом медленно возвращается ближе к исходному значению, когда система "отыгрывает" за счет газообмена, работы фильтра, органики.
- Буферная система стремится вернуться к заданному равновесию, поэтому небольшие внесения кислот/щелочей компенсируются и pH меняется гораздо меньше.
- Связь с KH:
- Голые кислоты преимущественно "съедают" KH, оставляя воду менее буферной и более нестабильной.
- Грамотный буфер, наоборот, обычно повышает или перестраивает KH, делая pH более предсказуемым.
Популярная схема: pH кажется слишком низким, берется "pH up", сода или другой щелочной препарат, и аквариумист поднимает значению до "красивых" цифр. Что идет не так:
- Подняли pH, но не учли аммиак. При высоком pH часть безопасного аммония NH4+ переходит в токсичный аммиак NH3. То, что было терпимо при pH 6,8, может стать опасным при pH 8,0 - без изменения показаний теста по "общему аммиаку".
- Резкий скачок pH - стресс для рыб. Для них важно не только абсолютное значение, но и скорость изменения. Переход с 6,8 до 7,8 за несколько часов эквивалентен для многих рыб "давлению в самолете": осморегуляция, работа жабр и ионный обмен нарушаются, иммунитет проседает.
- Система "отыгрывает назад". Если KH невысокий, дыхание рыб, бактерий, ночное накопление CO2 снова начнет тянуть pH вниз. Получается пила: то вверх химией, то вниз естественными процессами. Результат - вечные скачки и хронический стресс обитателей.
Откат - это когда после применения средства для повышения или понижения pH через день‑два значение почти возвращается к прежнему, а иногда даже "перелетает" в другую сторону.
Причины:
- Неперестроенный буфер. Карбонатная система воды все еще "настроена" на прежний диапазон, и пока вы силой сдвигаете pH, она пытается вернуть его туда, где ей "удобно".
- Газообмен с атмосферой. Если вы сильно изменили pH, но не изменили содержание CO2 закономерным образом, вода через некоторое время "подтянет" CO2 либо отдаст его, и pH снова сдвинется.
- Фильтрация и органика. Нитрификация, разложение отходов, выделение органических кислот - все это в итоге тянет pH вниз, особенно при слабом буфере.
Как работают буферные смеси для аквариума
Буферные препараты для пресной воды обычно:
- содержат карбонаты/гидрокарбонаты и другие соли, формирующие новый уровень KH;
- иногда включают слабо кислотные или слабо щелочные компоненты, задающие целевой диапазон pH (например, "pH 6,5-7,0" или "pH 7,5-8,0").
- меняет pH не "рывком", а плавно, по мере внесения и подмен;
- обеспечивает устойчивость - легкие колебания CO2, кормление, мелкие ошибки уже не вызывают резких скачков;
- задает "характер" воды под конкретный биотоп (мягкая слабокислая для тетр и дискусов или более щелочная и буферная для живородок и африканских цихлид).
Ключевой вывод: устойчивый pH - следствие состава воды, а не бутылочки "pH up/pH down".
Намного безопаснее и предсказуемее:
- задать нужный KH и GH: через осмос + реминерализация или подбор водопроводных источников;
- настроить газообмен и CO2 (если используется);
- избегать накопления органики, которая постепенно подтачивает буфер и ведет к "pH crash".
Когда буферные смеси действительно уместны
Буферные смеси имеют смысл, когда:
- вы сознательно формируете специфический биотоп (например, стабильная слабокислая вода для неонов и апистограмм);
- исходная вода нестабильна или крайне мягкая/жесткая, и требуется задать предсказуемый KH;
- используется осмос и нужно воспроизвести "одинаковую" воду от подмены к подмене.
Золотое правило регулировки pH
Вместо подхода "как сделать pH 7,0 любой ценой", гораздо продуктивнее мыслить так:
- какие рыбы и растения живут в аквариуме и какой диапазон pH для них нормален;
- каков реальный pH исходной воды и KH;
- можно ли добиться стабильных, пусть и неидеальных, параметров без ежедневной "химии";
- если вмешиваться - то через изменение буфера (KH, общая минерализация, газообмен), а не резкими вбросами кислот и щелочей.